2. 四川长宁竹林生态系统国家定位观测研究站,四川 宜宾 644000;
3. 中国林业科学研究院林业研究所,北京 100091
2. Changning Bamboo Forest Ecosystem Research Station, Yibin 644000, Sichuan, China;
3. Research Institute of Forestry, Chinese Academy of Forestry, Beijing 100091, China
毛竹(Phyllostachys edulis)是中国特有竹种,种植面积占中国竹林总面积的70%以上,在全球森林面积锐减的情况下,毛竹林面积仍以每年约3%的速度增加[1]。毛竹生长速度快和采伐周期短的生物学特性在缓解木材供需矛盾、调节气候变化中发挥重要的作用,但其爆发式生长不仅需要大量养分供给,高强度择伐作业和全竹利用也会限制养分归还,从而加剧造成毛竹林生态系统的养分限制[2]。芒萁(Dicranopteris dichoyoma)是毛竹林常见并广泛分布的林下植被,在粗放式经营毛竹林中呈强烈聚集分布的状态[3–4]。芒萁具有明显的磷元素富集特征[5–6],并可在林下迅速占领生长空间[7],说明其对土壤磷养分元素具有较强的获取能力,从而可能加剧目标树种的养分限制。尽管川南地区毛竹林生态系统是磷限制型生态系统,但毛竹林下的芒萁种群如何影响毛竹的养分限制还缺乏直接证据。
生态化学计量学能够指示对植物群落生产力起限制性作用的营养元素,近年来被广泛应用于评估植物营养状况和土壤对植物生长养分的供应情况。前人开展了芒萁群落对土壤化学计量特征影响的研究[8],但这些研究均将高度异质的土壤看作一个整体,忽略了土壤不同组成单元在养分供给中的作用。土壤团聚体是土壤无机矿物颗粒通过有机质的胶结和凝聚等作用形成土壤结构的基本组成单元[9],是调控土壤养分循环的主要场所。稳定的土壤团聚体结构可以调节土壤养分供需之间的矛盾, 保持土壤肥力的有效供给,进而维持植被生产力与土壤养分供给之间的密切联系[10]。前人研究发现植被类型是影响毛竹林土壤团聚体结构的主要因素,且多关注于不同团聚体粒径碳含量及其影响因素[11–13]。但关于毛竹林下植被对土壤团聚体氮磷养分特征的报道相对较少。因此限制了从生态化学计量学角度出发探究毛竹林土壤不同粒径团聚体养分循环的异质性。为此,本研究选择四川省长宁县粗放经营的毛竹林为研究对象,以毛竹林下不同盖度芒萁种群作为参考,探究芒萁种群对毛竹林土壤团聚体养分特征及其稳定性的影响,拟从毛竹林下植被管理和土壤养分状态的角度出发更好的指导毛竹林高效培育,促进毛竹林生态系统可持续经营。
1 材料和方法 1.1 研究区概况研究区位于四川省宜宾市长宁县蜀南竹海景区(28°15ʹ~28°47ʹ N,104°44ʹ~105°03ʹ E)的长宁竹林生态系统国家定位观测研究站内,该区位于云贵高原向四川盆地过渡区,处于西南丛生竹林区,江南混合竹和西南高山竹的分布交界区。该区属中亚热带湿润性季风气候,降水丰富,温暖湿润,年均降雨量1 114.2 mm,年均气温18.3 ℃。土壤以山地黄壤和紫色土为主(本研究所在区域属山地黄壤)[14]。该区域的竹种有毛竹、硬头黄竹(Bambusa rigida)、苦竹(Pleioblastus amarus)和慈竹(Neosinocalamus affinis)等。研究区内竹林主要为毛竹林,近10 a无复垦和施肥记录,林下植物主要以蕨类植被为主, 最常见芒萁集中连片分布,少量混杂狗脊(Wood-wardia japonica)和里白(Hicriopteris glaucum)等[15]。
1.2 样地设置2016年3月,选择立地条件基本一致,生长健壮、无病虫害的毛竹林,在林下芒萁盖度为7.75%的毛竹林内设置4个样方(PE);同时,在林下芒萁盖度为63.25%的毛竹林内设置4个样方(DD)。每个样方面积为20 m×20 m,样方间距为150 m以上,每个样方设置5个1 m×1 m的凋落物框,随机摆放在样方内,凋落物框距离地表高度1 m。2016年6月,在新竹成林后,对每个样方内所有毛竹进行株数统计,并对2016年新生竹每木检尺。2016年7月,在每个样方内随机设置5个5 m×5 m的亚样方并调查芒萁种群盖度(表 1)。
| 表 1 研究地基本情况 Table 1 Information of Phyllostachys edulis forest |
2016年7月,在各样方对角线交点处及距交点5 m处设置5个采样点,用剪刀剪断地表植被并轻轻去除,同时去除地表凋落物层。在每个采样点采集1个0~10 cm土层的原状土,将采集到的样品运回实验室并分拣其中的石子和植物残体。每个样品用尽量小的力沿土壤自然纹理掰开后过8 mm筛, 将相同样方的过筛样品多点混合后采用四分法取样, 一部分作为全土样品,室内风干后研磨过100目筛用于化学性质测定,一部分用于土壤团聚体颗粒分级。土壤团聚体颗粒分级采用干筛法[16–17]:土壤样品在4 ℃下风干至质量含水量约为15%以保证筛选效果,其中含水量测定为随机选择部分土壤样品烘干称重测定。每次称取100 g土壤样品置于震动筛分仪(Retsch AS200)中以1.5 mm振幅震动2 min, 获得大团聚体(> 2 mm)、中团聚体(0.25~2 mm)和微团聚体(< 0.25 mm) 3个团聚体粒径。分级后的土壤团聚体样品室内风干后研磨过100目筛用于化学性质测定。
毛竹凋落叶样品搜集于凋落物框,每个样方凋落物框内叶片混合均匀后带回实验室。同时,根据地表芒萁凋落叶颜色和形态搜集新鲜凋落叶样品。毛竹和芒萁细根样品(< 2 mm)搜集于原状土中,并用清水冲洗干净。所有植物样品65 ℃烘干后研磨过100目筛用于化学性质测定。
土壤和植物样品总有机碳(TOC)和全氮(TN)采用元素分析仪测定(ECS 4010 CHNSO, Costech Analytical Tecnologies Inc., Vlencia, CA, USA),土壤和植物样品全磷(TP)用H2SO4/HClO4消煮后采用化学分析仪测定(Smartchem 300, AMS-AllianceWestco Scientific Instruments, Rome, Italy)[18]。
1.4 数据处理土壤团聚体含量采用质量百分含量计算[19], Wi=Ji/K, 式中, Wi为某粒径范围团聚体含量(%),Ji为某粒径范围团聚体干重,K为用于筛分团聚体的土壤样品总重。
土壤团聚体平均质量直径(mean weight diameter, MWD)=
采用t检验比较2种类型样方林下盖度、立竹株数、新生竹株数和新生竹胸径间的差异,采用t检验比较2种类型样方毛竹和芒萁凋落叶和细根以及土壤相同团聚体粒径的化学性质和化学计量比的差异,采用单因素方差分析比较相同样方内不同团聚体粒径土壤化学性质及化学计量比之间的差异,采用方差分解解析不同粒径团聚体化学性质对土壤化学性质的贡献,采用Pearson法进行土壤和植物样品C、N、P含量的相关性分析,采用SPSS 16.0统计分析软件对数据进行差异性检验(显著性检验水平以P < 0.05表示具有显著性差异),采用SigmaPlot 12.5软件制图。
2 结果和分析 2.1 凋落叶和细根主要养分化学计量特征与PE样方相比,芒萁并未影响DD样方中毛竹凋落叶和细根的TOC、TN和TP含量以及C: N、C: P和N: P,但芒萁与毛竹凋落叶和细根的化学性质及化学计量特征差异显著(表 2)。芒萁细根的TOC含量显著低于毛竹细根,但前者凋落叶和细根的TN和TP含量显著高于毛竹。因此,芒萁凋落叶和细根的C: N、C: P和N: P均低于毛竹(除细根N: P外) (表 2)。
| 表 2 毛竹和芒萁凋落叶和细根的主要养分含量及化学计量比 Table 2 Nutrient contents and stoichiometry in litter leaves and fine roots of Phyllostachys edulis and Dicranopteris dichoyoma |
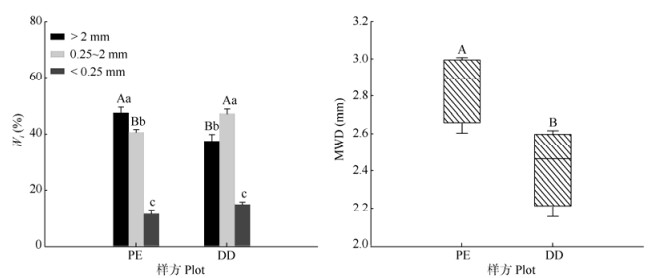
DD与PE相比,土壤大团聚体含量显著降低,中团聚体含量显著提高,对微团聚体含量无影响(图 1)。DD和PE土壤团聚体分布呈明显差异,具体表现为PE中3种团聚体含量呈现从大团聚体到微团聚体逐渐降低,且差异极显著(P < 0.01);而DD中3种团聚体含量呈现中团聚体含量显著高于大团聚体和微团聚体。除团聚体含量外,MWD在2个样方间差异显著,PE中MWD显著高于DD样方。
|
图 1 毛竹林不同样方的土壤团聚体含量(Wi)和平均质量直径(MWD)。柱上不同大、小写字母分别表示相同团聚体粒径不同样方间和相同样方不同团聚体粒径间差异显著(P < 0.05)。下同 Fig. 1 Aggregate contents (Wi) and mean weight diameter (MWD) in different plots of Phyllostachys edulis forest. Different capital and small letters upon column indicate significant differences between PE and DD plots within the same aggregate diameter and among different aggregate diameter in the same plots at 0.05 level, respectively. The same below |
从表 3可见,PE样方土壤的TOC (P=0.04)、TN (P=0.02)和TP (P < 0.01)含量均显著高于DD样方; DD样方的TP含量降低了(66.01±17.99)%,TOC和TN含量分别降低了(10.84±4.61)%和(21.82±5.24)%, TP的下降幅度显著高于TOC和TN,从而导致DD样方土壤的C: N、C: P和N: P显著增加, C: N增加了(8.81±3.20)%,N: P和C: P分别增加了(23.76± 9.36)%和(31.21±6.20)%,C: N增加幅度显著低于C: P。
| 表 3 不同样方土壤的养分含量及化学计量比 Table 3 Soil nutrient contents and stoichiometry in different plots |
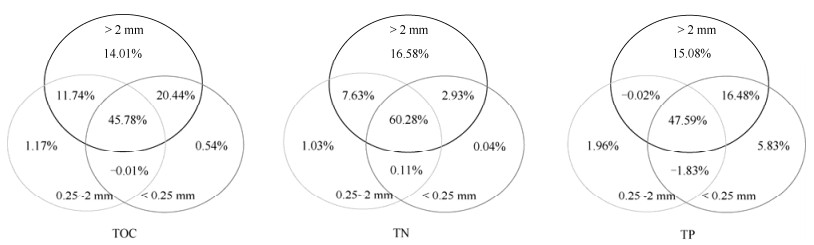
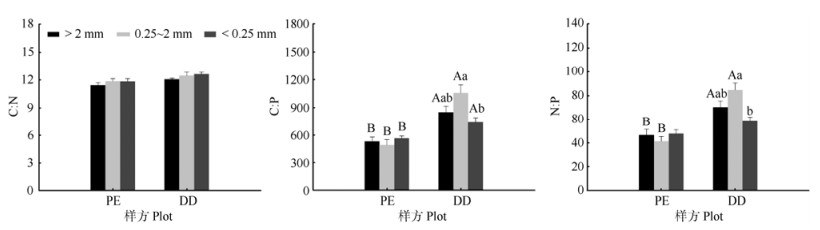
与PE样方相比,DD样方土壤中3种团聚体粒径的TP含量均显著降低,但仅大团聚体和中团聚体TN含量和大团聚体TOC含量显著降低(图 2)。同时,PE和DD样方中不同粒径团聚体TOC、TN和TP含量呈显著差异,具体为PE样方3种团聚体TOC、TN和TP含量无差异;而DD样方3种团聚体TOC、TN和TP含量均呈现随团聚体粒径减少而增加的趋势,其中微团聚体TOC和TP含量均显著高于大团聚体,中团聚体也显著高于大团聚体。方差分析表明:大团聚体TOC、TN和TP对土壤TOC、TN和TP的贡献均高于中团聚体和微团聚体(图 3)。PE和DD样方中不同粒径团聚体的C: N无显著差异,但DD样方中不同粒径团聚体C: P和N: P显著高于PE样方(除微团聚体的N: P外)(图 4)。

|
图 2 不同样方毛竹林土壤团聚体的养分含量。TOC: 总有机碳; TN: 全氮; TP: 全磷。 Fig. 2 Nutrient contents of soil aggregate in different plots. TOC: Total organic carbon; TN: Total nitrogen; TP: Total phosphorus. |
|
图 3 不同粒径团聚体养分含量对土壤的贡献 Fig. 3 Nutrient content contribution of different aggregate diameter to soil |
|
图 4 不同样方土壤团聚体的化学计量特征 Fig. 4 Stoichiometry characters of soil aggregate in different plots |
由表 4可知,PE样方中毛竹凋落叶的TP含量与微团聚体的TN含量呈显著正相关(P=0.008),而DD样方中毛竹凋落叶的TN含量与大团聚体和微团聚体的TP含量呈显著正相关(P=0.033, P=0.015),芒萁凋落叶的TN含量与微团聚体的TN含量呈显著正相关(P=0.006)。PE样方中毛竹细根的TN含量与中团聚体和微团聚体的TN含量呈显著正相关(P= 0.028, P=0.022),毛竹细根的TP含量与大团聚体的TP含量呈显著正相关(P=0.004);而DD样方中毛竹细根的TP含量与大团聚体和微团聚体的TP含量呈显著正相关(P=0.042, P=0.011),芒萁细根的TP含量与大团聚体和中团聚体的TP含量呈显著正相关(P=0.019, P=0.013)。
| 表 4 凋落叶和细根化学性质与土壤团聚体化学性质的相关性 Table 4 Correlations of chemical properties between soil aggregate and litter leaves, fine roots of Phyllostachys edulis and Dicranopteris dichoyoma |
作为土壤团聚体稳定性的综合体现,MWD越大表示团聚体平均粒径的团聚程度越高,团聚体稳定性越强[20]。本研究中DD样方MWD比PE样方显著降低14.9%,说明芒萁种群导致毛竹林土壤团聚体稳定性降低。这种团聚体稳定性的降低主要是因为大团聚体的裂解以及中小团聚体的形成。前人[21–22]研究表明植物根系直接或者通过与外生菌丝结合间接改变土壤团聚体组成。芒萁作为研究地内毛竹林下的优势群落,其根系在林下迅速生长以保证其种群在与乔木层树种竞争中对光、水分和养分的获取[7]。根系在生长过程中主要破坏大团聚体结构[22],从而导致团聚体结构从大团聚体向中小团聚体转变[23]。任立宁等[24]研究表明DD样方具有大量的芒萁细根,故可以支持这种解释。此外,土壤有机质在维持土壤团聚体稳定性中发挥胶结的作用,土壤有机质分解后会促进大粒径团聚体向小粒径团聚体转化[25–26]。DD样方大团聚体TOC含量显著低于PE,也可能是导致前者团聚体结构变化的重要原因。
3.2 芒萁种群对土壤团聚体养分特征的影响本研究表明,芒萁种群显著降低了土壤TOC含量,这可能是由于芒萁细根增加了土壤非毛管孔隙度,提高土壤通气性[24],进而促进土壤微生物对土壤有机碳的分解作用。DD样方大团聚体TOC含量显著低于PE样方,而中团聚体和微团聚体TOC含量在2个样地间差异不显著,这是由于土壤大团聚体有机碳比微团聚体有机碳更易矿化分解[27]。方差分析进一步表明大团聚体对土壤有机碳的影响(14.01%)高于中团聚体(1.17%)和微团聚体(0.54%), 因此大团聚体TOC含量降低是导致土壤TOC含量降低的主要原因。前期研究表明,该区域毛竹和芒箕凋落叶混合分解对有机碳释放表现为负效应[28], 芒萁群落限制了毛竹林凋落叶分解过程中有机碳向土壤的归还,因此芒萁群落引起土壤TOC含量降低。此外,芒萁较高的细根N浓度可形成N-木质素络合物抑制细根分解作用[29],芒萁较细的细根也可抑制细根分解作用[30],使其分解速率显著低于毛竹细根分解速率[15],因此芒萁群落可能会降低其细根有机碳在参与土壤TOC形成中的贡献,进而引起DD样方土壤TOC低于PE样方。
除土壤TOC外,芒萁种群显著降低了土壤的TN含量,方差分析结果表明大团聚体对土壤全氮的影响(16.58%)高于中团聚体(1.03%)和微团聚体(0.04%),因此大团聚体TN含量降低是引起土壤TN降低的主要原因。毛竹的速生特性促使其将大量的营养元素储存在茎秆中,长期的采伐作业限制了该区域毛竹林生态系统养分内循环过程,大量养分随采伐作业从生态系统输出且不能得到及时的补偿[2]。与毛竹相比,芒萁凋落叶和细根具有较高的TN含量,这是由于芒萁种群通过养分竞争作用与乔木层植物争夺更多的土壤氮素以供自身的生长和发育[31–32], 导致土壤TN含量降低。与土壤TOC和TN含量相同,芒萁种群显著降低了土壤TP含量, 且DD样方土壤TP含量下降量显著高于土壤TOC和TN含量下降量,说明毛竹林下的芒萁种群导致土壤TP含量降低更为明显。在不同团聚体粒径中,TOC含量仅在大团聚体呈现显著差异,TN含量仅在中团聚体和微团聚体呈现显著差异,而TP含量在大团聚体、中团聚体和微团聚体均呈现显著差异。Wang等[10]研究表明土壤大团聚体磷的解吸附作用高于微团聚体,进而导致大团聚体中的磷元素更优先被植被根系吸收利用。本研究也表明毛竹和芒萁细根TP含量均与土壤大团聚体TP含量显著正相关,说明毛竹和芒萁均利用土壤大团聚体中的TP。方差分析结果也进一步表明了大团聚体更多的影响土壤TP含量,说明芒萁种群对土壤大团聚体中磷元素的吸收利用是DD样方TP含量降低的主要原因。此外,PE样方毛竹细根TP仅与土壤大团聚体TP含量显著正相关,而DD样方毛竹细根TP与微团聚体TP含量显著正相关,且芒萁细根TP与中团聚体TP含量显著正相关,这可能是因为芒萁具有较高的磷利用效率[6],在与其他植物的养分竞争中具有较强的磷元素竞争能力[33]。DD样方芒萁种群可能加剧了与毛竹对磷元素的竞争,因此毛竹和芒萁的细根分别需要从微团聚体和中团聚体中吸收磷,故导致DD样方微团聚体和中团聚体TP含量显著低于PE样方。
3.3 芒萁种群对土壤团聚体化学计量特征的影响芒萁种群导致土壤C: N、C: P和N: P显著提高,对比不同粒径团聚体化学计量特征分析表明,芒萁种群并未显著改变不同粒径团聚体C: N,但显著提高了不同粒径团聚体土壤C: P和N: P (除微团聚体N: P外)。与TOC和TN相比,DD样方土壤团聚体TP含量下降更多,这是因为试验地属于磷限制型生态系统[18],芒萁种群与毛竹对磷元素的竞争作用要强于对氮元素的竞争作用。虽然本研究表明DD样方土壤大团聚体和中团聚体的TN显著低于PE,但DD样方土壤大团聚体和中团聚体N: P仍显著高于PE,说明与芒萁种群引起大团聚体和中团聚体TN含量降低相比,芒萁种群引起大团聚体和中团聚体TP含量降低更多,这是因为二者在共同利用大团聚体TP的同时,芒萁也利用了中团聚体的TP。Güsewell[34]研究表明植物叶片N: P > 16时,生态系统受磷限制。本研究中毛竹与芒萁凋落叶和细根N: P为83.5~108.2,说明该区域毛竹和芒萁同时受到土壤磷元素的限制作用[18]。芒萁种群引起土壤N: P显著提高会进一步加剧其与毛竹对磷元素的竞争作用。土壤C: P作为衡量土壤磷有效性的指标, C: P越低土壤磷有效性越高[35]。DD样方的大团聚体、中团聚体和微团聚体C: P显著高于PE样方, 进一步说明了芒萁加剧了土壤磷元素的限制作用。生长率假说认为快速生长的生物个体需要合成大量的核糖体,核糖体在合成蛋白质过程中需要磷元素作为结构支撑,因此磷元素在毛竹生长发育过程中具有重要的作用[2, 36–37],土壤磷有效性的降低会限制毛竹生长,这可能是DD毛竹新生竹胸径显著低于PE样方的重要原因。
综上,川南地区毛竹林下高盖度的芒萁种群显著改变了土壤团聚体组成,降低了毛竹林土壤团聚体稳定性。芒萁种群通过降低土壤大团聚体TOC、TN和TP含量导致土壤TOC、TN和TP含量降低,进而提高了土壤C: N、C: P和N: P。此外,高盖度的芒萁种群显著降低了土壤中、小团聚体的TP含量,这可能是因为土壤大团聚体磷元素的限制作用促进了毛竹和芒萁根系对中、小团聚体TP的吸收和利用。因此,在川南地区粗放经营毛竹林中应适宜考虑调整林下芒萁盖度,在保证不加剧水土流失的前提下尽量降低芒萁与毛竹的养分竞争,尤其是对磷元素的竞争,进而提升毛竹林生产力。
| [1] |
WANG B, WEI W J, LIU C J, et al. Biomass and carbon stock in moso bamboo forests in subtropical China: Characteristics and implications[J]. J Trop For Sci, 2013, 25(1): 137-148. |
| [2] |
LIU G L. Study on the mechanism of maintaining long-term productivity of bamboo forest [D]. Beijing: Chinese Academy of Forestry, 2009. 刘广路. 毛竹林长期生产力保持机制研究[D]. 北京: 中国林业科学研究院, 2009. |
| [3] |
FAN Y R, CHEN S L, LIN H, et al. Effects of different disturbance measures on spatial distribution patterns of understory plants in Phyllostachys edulis forests[J]. Biod Sci, 2013, 21(6): 709-714. 樊艳荣, 陈双林, 林华, 等. 不同林下植被干扰措施对毛竹林下植物种群分布格局的影响[J]. 生物多样性, 2013, 21(6): 709-714. DOI:10.3724/sp.j.1003.2013.06020 |
| [4] |
PAN B Z. An experiment on chemically preventing and killing off weeds mainly consisting of Dicranopteris linearis in bamboo forests[J]. J Fujian For Sci Technol, 2000, 27(2): 76-78. 潘标志. 竹林化学防除芒萁骨为主杂草试验[J]. 福建林业科技, 2000, 27(2): 76-78. DOI:10.13428/j.cnki.fjlk.2000.02.021 |
| [5] |
CHEN J, ZHONG Z C. Characteristics of nutrient elements cycling in fern community[J]. Acta Ecol Sin, 1991, 11(4): 299-306. 陈建, 钟章成. 芒萁群落中营养元素的循环特点[J]. 生态学报, 1991, 11(4): 299-306. |
| [6] |
GUAN D S. Nutrient utilization efficiency of grassland, fernland and shrubland in Hong Kong[J]. Chin J Ecol, 1995, 14(2): 23-26. 管东生. 香港草地、芒萁和灌木群落的养分利用效率[J]. 生态学杂志, 1995, 14(2): 23-26. |
| [7] |
WANG X L, ZHAO J, WU J P, et al. Impacts of understory species removal and/or addition on soil respiration in a mixed forest plantation with native species in southern China[J]. For Ecol Manag, 2011, 261(6): 1053-1060. DOI:10.1016/j.foreco.2010.12.027 |
| [8] |
CHEN J J, CHEN Z B, CHEN Z Q, et al. Dicranopteris dichotoma leaf stoichiometry in collapsing erosion areas in southwest Fujian[J]. Chin J Eco-Agric, 2018, 26(11): 1710-1719. 陈俊佳, 陈志彪, 陈志强, 等. 闽西南崩岗侵蚀区芒萁叶片生态化学计量特征[J]. 中国生态农业学报, 2018, 26(11): 1710-1719. DOI:10.13930/j.cnki.cjea.180580 |
| [9] |
NIE M, PENDALL E, BELL C, et al. Soil aggregate size distribution mediates microbial climate change feedbacks[J]. Soil Biol Biochem, 2014, 68: 357-365. DOI:10.1016/j.soilbio.2013.10.012 |
| [10] |
WANG X, YOST R S, LINQUIST B A. Soil aggregate size affects phosphorus desorption from highly weathered soils and plant growth[J]. Soil Sci Soc Am J, 2001, 65(1): 139-146. DOI:10.2136/sssaj2001.651139x |
| [11] |
YU L, XU H N, XIAO F M, et al. The characters of soil aggregate organic carbon under different types of Phyllostachys edulis forest[J]. Acta Agric Univ Jiangxi (Nat Sci), 2017, 39(4): 713-720. 余林, 徐海宁, 肖复明, 等. 不同类型毛竹林土壤团聚体有机碳特征研究[J]. 江西农业大学学报, 2017, 39(4): 713-720. DOI:10.13836/j.jjau.2017093 |
| [12] |
XIAO F M, FAN S H, WANG S L, et al. Moso bamboo plantation soil aggregate stability and its impact on carbon storage[J]. J Soil Water Conserv, 2008, 22(2): 131-134. 肖复明, 范少辉, 汪思龙, 等. 毛竹林地土壤团聚体稳定性及其对碳贮量影响研究[J]. 水土保持学报, 2008, 22(2): 131-134. DOI:10.3321/j.issn:1009-2242.2008.02.030 |
| [13] |
YOU X H. A study on the effect of soil aggregate on organic matter in mixed forests of Chinese fir and Phyllostachys heterocycla cv. pubescens[J]. Acta Agric Univ Jiangxi, 2004, 26(4): 536-539. 游秀花. 杉木毛竹混交林土壤团聚体对有机质含量的影响分析[J]. 江西农业大学学报, 2004, 26(4): 536-539. DOI:10.3969/j.issn.1000-2286.2004.04.013 |
| [14] |
GAO Q W, DAI B, LUO C D, et al. Spatial heterogeneity of soil physical properties in Phyllostachys heterocycla cv. pubescens forest, south Sichuan Bamboo Sea[J]. Acta Ecol Sin, 2016, 36(8): 2255-2263. 高强伟, 代斌, 罗承德, 等. 蜀南竹海毛竹林土壤物理性质空间异质性[J]. 生态学报, 2016, 36(8): 2255-2263. DOI:10.5846/stxb201410061961 |
| [15] |
REN L N, LIU S R, CAI C J, et al. Decomposition characteristics of the fine root of Phyllostachys edulis and Dicranopteris pedata in southern Sichuan[J]. Acta Ecol Sin, 2018, 38(21): 7638-7646. 任立宁, 刘世荣, 蔡春菊, 等. 川南地区毛竹和林下植被芒箕细根分解特征[J]. 生态学报, 2018, 38(21): 7638-7646. DOI:10.5846/stxb201801200158 |
| [16] |
DORODNIKOV M, BLAGODATSKAYA E, BLAGODATSKY S, et al. Stimulation of microbial extracellular enzyme activities by elevated CO2 depends on soil aggregate size[J]. Glob Change Biol, 2009, 15(6): 1603-1614. DOI:10.1111/j.1365-2486.2009.01844.x |
| [17] |
JING Y L, LIU S R, YIN Y, et al. Effects of N-fixing tree species (Alnus sibirica) on amino sugars in soil aggregates of Larix kaempferi plantation in eastern Liaoning Province, China[J]. Chin J Appl Ecol, 2018, 29(6): 1753-1758. 井艳丽, 刘世荣, 殷有, 等. 引入固氮树种对辽东落叶松人工林土壤团聚体氨基糖的影响[J]. 应用生态学报, 2018, 29(6): 1753-1758. DOI:10.13287/j.1001-9332.201806.020 |
| [18] |
GAO X M, LIU S R, WANG Y, et al. Effects of throughfall reduction and nitrogen addition on stoichiometry of leaf and fine root in Phyllostachys edulis forests[J]. Acta Ecol Sin, 2021, 41(4): 1440-1450. 高小敏, 刘世荣, 王一, 等. 穿透雨减少和氮添加对毛竹叶片和细根化学计量学的影响[J]. 生态学报, 2021, 41(4): 1440-1450. DOI:10.5846/stxb202003260704 |
| [19] |
LEI L, XIAO W F, ZENG L X, et al. Distribution of enzymatic activities within soil aggregates in two types of Pinus massoniana mixed plantations in the Three Gorges Reservoir area[J]. Acta Ecol Sin, 2020, 40(17): 6179-6188. 雷蕾, 肖文发, 曾立雄, 等. 三峡库区2种马尾松混交林土壤团聚体酶活性分布特征[J]. 生态学报, 2020, 40(17): 6179-6188. DOI:10.5846/stxb201912252783 |
| [20] |
CHENG M, ZHU Q L, LIU L, et al. Effects of vegetation on soil aggregate stability and organic carbon sequestration in the Ningxia Loess Hilly Region of northwest China[J]. Acta Ecol Sin, 2013, 33(9): 2835-2844. 程曼, 朱秋莲, 刘雷, 等. 宁南山区植被恢复对土壤团聚体水稳定及有机碳粒径分布的影响[J]. 生态学报, 2013, 33(9): 2835-2844. DOI:10.5846/stxb201202090169 |
| [21] |
CHENG M, XIANG Y, XUE Z J, et al. Soil aggregation and intraaggregate carbon fractions in relation to vegetation succession on the Loess Plateau, China[J]. Catena, 2015, 124: 77-84. DOI:10.1016/j.catena.2014.09.006 |
| [22] |
JASTROW J D, MILLER R M, LUSSENHOP J. Contributions of interacting biological mechanisms to soil aggregate stabilization in restored prairie[J]. Soil Biol Biochem, 1998, 30(7): 905-916. DOI:10.1016/S0038-0717(97)00207-1 |
| [23] |
LENKA N K, CHOUDHURY P R, SUDHISHRI S, et al. Soil aggregation, carbon build up and root zone soil moisture in degraded sloping lands under selected agroforestry based rehabilitation systems in eastern India[J]. Agric Ecosys Environ, 2012, 150: 54-62. DOI:10.1016/j.agee.2012.01.003 |
| [24] |
REN L N. Study on soil organic carbon and soil microbes in moso bamboo forests in Southern Sichuan[D]. Beijing: Chinese Academy of Forestry, 2018. 任立宁. 川南毛竹林土壤有机碳和土壤微生物研究[D]. 北京: 中国林业科学研究院, 2018. |
| [25] |
OADES J M. Soil organic matter and structural stability: Mechanisms and implications for management[J]. Plant Soil, 1984, 76(12/3): 319-337. DOI:10.1007/BF02205590 |
| [26] |
ZHANG M K, HE Z L, CHEN G C, et al. Formation of water-stable aggregates in red soils as affected by land use[J]. Acta Pedol Sin, 1997, 34(4): 359-366. 章明奎, 何振立, 陈国潮, 等. 利用方式对红壤水稳定性团聚体形成的影响[J]. 土壤学报, 1997, 34(4): 359-366. |
| [27] |
ELLIOTT E T, CAMBARDELLA C A. Physical separation of soil organic matter[J]. Agric Ecosys Environ, 1991, 34(1-4): 407-419. DOI:10.1016/0167-8809(91)90124-G |
| [28] |
REN L N, LIU S R, WANG Y, et al. Decomposition characteristics of litter of Phyllostachys edulis and Dicranopteris pedata[J]. For Res, 2018, 31(5): 91-97. 任立宁, 刘世荣, 王一, 等. 毛竹和林下植被芒箕凋落物分解特征研究[J]. 林业科学研究, 2018, 31(5): 91-97. DOI:10.13275/j.cnki.lykxyj.2018.05.012 |
| [29] |
CAMIRÉ C, CÔTÉ B, BRULOTTE S. Decomposition of roots of black alder and hybrid poplar in short-rotation plantings: Nitrogen and lignin control[J]. Plant Soil, 1991, 138(1): 123-132. DOI:10.1007/BF00011814 |
| [30] |
MCCLAUGHERTY C A, ABER J D, MELILLO J M. Decomposition dynamics of fine roots in forested ecosystems[J]. Oikos, 1984, 42(3): 378-386. DOI:10.2307/3544408 |
| [31] |
CUI N J. Effect of gap size on plant diversity and stoichiometric characteristics of dominant species in Pinus massoniana plantation[D]. Chengdu: Sichuan Agricultural University, 2014. 崔宁洁. 林窗大小对马尾松人工林林下植物多样性及优势种化学计量特征的影响[D]. 成都: 四川农业大学, 2014. |
| [32] |
ZHOU Y, ZHANG D J, SONG S M, et al. Forest gaps size on Pinus massoniana plantation of three natural regeneration herb N and P stoichiometry[J]. Bull Bot Res, 2017, 37(6): 915-925. 周扬, 张丹桔, 宋思梦, 等. 林窗大小对马尾松林下3种更新草本植物N、P化学计量研究[J]. 植物研究, 2017, 37(6): 915-925. DOI:10.7525/j.issn.1673-5102.2017.06.015 |
| [33] |
CHEN J Q, ZHANG L L, LI J, et al. Carbon, nitrogen and phosphorus stoichiometry of two fern species and their relationships to nutrient availability[J]. J Trop Subtrop Bot, 2014, 22(6): 567-575. 陈嘉茜, 张玲玲, 李炯, 等. 蕨类植物碳氮磷化学计量特征及其与土壤养分的关系[J]. 热带亚热带植物学报, 2014, 22(6): 567-575. DOI:10.11926/j.issn.1005-3395.2014.06.004 |
| [34] |
GÜSEWELL S. N: P ratios in terrestrial plants: Variation and functional significance[J]. New Phytol, 2004, 164(2): 243-266. DOI:10.1111/j.1469-8137.2004.01192.x |
| [35] |
WANG S Q, YU G R. Ecological stoichiometry characteristics of ecosystem carbon, nitrogen and phosphorus elements[J]. Acta Ecol Sin, 2008, 28(8): 3937-3947. 王绍强, 于贵瑞. 生态系统碳氮磷元素的生态化学计量学特征[J]. 生态学报, 2008, 28(8): 3937-3947. DOI:10.3321/j.issn:1000-0933.2008.08.054 |
| [36] |
ELSER J J, DOBBERFUHL D R, MACKAY N A, et al. Organism size, life history, and N: P stoichiometry: Toward a unified view of cellular and ecosystem processes[J]. Bioscience, 1996, 46(9): 674-684. DOI:10.2307/1312897 |
| [37] |
ELSER J J, FAGAN W F, KERKHOFF A J, et al. Biological stoichiometry of plant production: Metabolism, scaling and ecological response to global change[J]. New Phytol, 2010, 186(3): 593-608. DOI:10.1111/j.1469-8137.2010.03214.x |
 2023, Vol. 31
2023, Vol. 31



