2. 中国热带农业科学院热带生物技术研究所/海南省黎药资源天然产物研究与利用重点实验室, 海口 571101
2. Hainan Key Laboratory for Research and Development of Natural Products from Li Folk Medicine, Institute of Tropical Bioscience and Biotechnology, Chinese Academy of Tropical Agricultural Sciences, Haikou 571101, China
兰科 (Orchidaceae) 石斛属 (Dendrobium) 全世界约有1000余种,广泛分布于亚热带和热带地区至大洋洲,中国有74种,主产西南及华南地区[1],其中大约40种被作为药用[2],如铁皮石斛 (D. officinale Kimura et Migo) 和金钗石斛 (D. nobile Lindl.) 等。兰科石斛属植物多数因其花色鲜艳奇特,气味芳香, 具有较高的园艺价值;石斛的药用化学成分主要是石斛碱、联苄类、菲类和多糖[3]等物质,其药用价值[4]及保健功能主要有以下几个方面:治疗胃阴不足,病后虚热不退,目暗不明[5]、糖尿病[6-8]等症。同时现代药理实验也证明,石斛对抑制肿瘤细胞生长等方面都具有显著疗效,对增强人体免疫力、抗氧化、抗衰老均具有明显作用[9],受到国内外学者的广泛关注[10]。
华石斛 (Dendrobium sinense T. Tang et F. T. Wang) 为海南特有种,仅产于中国海南 (保亭、乐东、白沙和琼中等县)[11],因其附生于海拔1000 m的山地疏林中树干上,对温度、湿度、光照等自然条件都具有较高要求,且种子萌发率较低,导致华石斛资源稀缺,也因此华石斛化学成分研究环节长期薄弱。
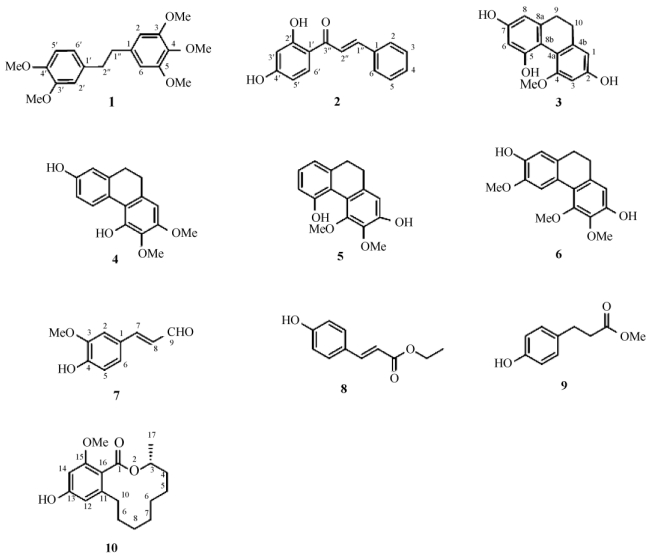
本文对华石斛乙醇提取物进行了系统的化学成分研究,利用现代色谱技术和波谱技术分离鉴定了10个化合物,分别是鼓槌石斛素 (1)、2′, 4′-二羟基查尔酮 (2)、2, 5, 7-三羟基-4-甲氧基-9, 10-二氢菲 (3)、4, 7-二羟基-2, 3-二甲氧基-9, 10-二氢菲 (4)、2, 5-二羟基-3, 4-二甲氧基-9, 10-二氢菲 (5)、2, 7-二羟基-3, 4, 6-三甲氧基-9, 10-二氢菲 (6)、(E) 松柏醛 (7)、反式对羟基肉桂酸酯 (8)、对羟基苯丙酸甲酯 (9) 和十二元内环酯 (10)(图 1)。其中化合物1~10均为首次从华石斛中分离得到。
|
图 1 化合物1~10的结构 Fig. 1 Structures of compounds 1-10 |
Bruker AM-400核磁共振光谱仪,Waters XEVO 7Q-S型质谱仪,DIONEX SUMMIT高校液相色谱仪,青岛美高公司生产的柱色谱硅胶 (200~300目) 和薄层色谱硅胶GF254,RS-232(20L) Heidolph Elektro GmbH & Co大旋转蒸发仪,GE Biosciences公司生产的Sephadex LH-20,日本YMC公司生产的反相硅胶ODS C-8,薄层色谱TLC显色为10% H2SO4乙醇显色剂,喷板后小火慢烤。乙酰胆碱酯酶购自Solarbio公司;4-硝基苯基-α-d-吡喃葡萄糖苷 (PNPG)、碘化硫代乙酰胆碱;ELX-800酶标仪购自美国宝特公司。
华石斛 (全草) 于2015年11月采自海南霸王岭,由海南大学园艺园林学院宋希强教授鉴定为兰科 (Orchidaceae) 石斛属华石斛 (Dendrobium sinense T. Tang et F. T. Wang),标本 (编号为TCY20151109) 存放于海南大学园艺园林学院。
1.2 提取分离华石斛全草 (8.0 kg) 晒干粉碎后,用95%乙醇 (20 L) 于80℃水浴提取3次,每次热回流3 h,减压浓缩提取液得到浸膏。依次用石油醚、乙酸乙酯及正丁醇萃取,得到乙酸乙酯部分浸膏80.0 g。
将乙酸乙酯浸膏用硅胶 (200~300目) 柱色谱分离,以石油醚-乙酸乙酯[8:2~2:8,V/V, 下同]混合溶剂梯度洗脱,得到8个馏分 (Fr.1~Fr.8)。Fr.1 (10.2 g) 经MCI层析,甲醇洗脱,除去叶绿素后, 再经固定相为ODS C-8反相键合硅胶,以水-甲醇 (7:3~1:9) 混合溶剂梯度分段,经硅胶柱色谱石油醚-乙酸乙酯 (8:2~2:8) 梯度洗脱分离得到化合物6 (5.7 mg)、4 (16.2 mg)、7 (4.0 mg) 和8 (30.1 mg)。Fr.2 (8.6 g) 经MCI层析,甲醇洗脱,除去叶绿素后,再经固定相为ODS C-8反相键合硅胶,以水-甲醇 (9:1~1:9) 混合溶剂梯度分段,经硅胶柱色谱石油醚-乙酸乙酯 (7:1~3:1) 梯度洗脱后,再经Sephadex LH-20 (甲醇) 洗脱分离到化合物5 (2.0 mg) 和9 (12.0 mg)。Fr.3 (16.5 g) 经MCI层析, 甲醇洗脱,除去叶绿素后,再经固定相为ODS C-8反相键合硅胶,以水-甲醇 (8:2~1:9) 混合溶剂梯度分段,经硅胶柱色谱石油醚-乙酸乙酯 (9:1~3:7) 梯度洗脱后,再经Sephadex LH-20 (甲醇) 洗脱分离到化合物1 (20.0 mg)、3 (7.5 mg)、10 (20.0 mg) 和2 (3.0 mg)。
1.3 结构鉴定鼓槌石斛素 (Chrysotoxine, 1) 无色针状晶体,ESI-MS m/z: [M + Na]+ 355,分子式C19H24O5。1H NMR (CDCl3, 500 MHz): δ 7.00 (1H, d, J=2.14 Hz, H-2′), 6.75 (1H, d, J=9 Hz, H-5′), 6.64 (1H, dd, J=9, 2.14 Hz, H-6′), 6.39 (2H, s, H-2, 6), 3.76 (9H, s, 3/4/5-OMe), 3.71 (3H, s, 3′-OMe), 3.71 (3H, s, 4′-OMe) 2.75 (4H, s, H-1′′, 2′′); 13C NMR (CDCl3, 125 MHz): δ 139.3 (s, C-1), 106.8 (d, C-2/6), 144.5 (s, C-3/5), 134.6 (s, C-4), 137.0 (s, C-1′), 110.2 (d, C-2′), 143.5 (s, C-3′), 148.3 (s, C-4′), 113.5 (d, C-5′), 110.2 (d, C-6′), 39.0 (q, C-1′′), 38.7 (q, C-2′′), 56.3 (q, 3-OMe), 56.3 (q, 4-OMe), 56.5 (q, 5-OMe), 56.3 (q, 3′-OMe), 56.3 (q, 4′-OMe)。以上数据与文献[12]报道基本一致,故鉴定该化合物1为鼓槌石斛素。
2′, 4′-二羟基查尔酮 (2′, 4′-Dihydroxy chalcone, 2) 白色无定形粉末,ESI-MS m/z: [M + Na]+ 263,分子式C15H12O3。1H NMR (CDCl3, 500 MHz): δ 8.74 (s, 2′-OH), 8.35(s, 4′-OH), 8.17 (1H, d, J=15.1 Hz, H-1′′), 7.97 (1H, d, J=16 Hz, H-2′′), 7.87 (2H, m, J=7.8 Hz, H-3/5), 7.74 (2H, m, H-2/6), 7.52 (1H, m, H-2′), 7.48 (1H, m, H-5′), 7.44 (1H, m, H-6′), 6.50 (1H, d, J=8.0 Hz, H-4); 13C NMR (CDCl3, 125 MHz): δ 136.4 (s, C-1), 130.1 (d, C-2/6), 129.7 (d, C-3/5), 131.6 (d, C-4), 114.4 (s, C-1′), 167.0 (s, C-2′), 104.0 (d, C-3′), 165.9 (s, C-4′), 109.7 (d, C-5′), 133.6 (d, C-6′), 121.9 (d, C-1′′), 145.0 (d, C-2′′), 193.2 (s, C-3′′)。以上数据与文献[13]报道基本一致,故鉴定该化合物2为2′, 4′-二羟基查尔酮。
2, 5, 7-三羟基-4-甲氧基-9, 10-二氢菲 (2, 5, 7-Trihydroxy-4-methoxy-9, 10-dihydrophenanthrene, 3) 红色无定形粉末,ESI-MS m/z: [M + Na]+ 281,分子式C15H14O4。1H NMR (CDCl3, 500 MHz): δ 6.50 (1H, d, J=2.34 Hz, H-8), 6.45 (1H, d, J=2.34 Hz, H-6), 6.31 (1H, d, J=2.51 Hz, H-1), 6.26 (2H, d, J=2.51 Hz, H-3), 3.88 (3H, s, 4-OMe), 2.56 (4H, s, H-9/10); 13C NMR (CDCl3, 125 MHz): δ 110.2 (d, C-1), 158.0 (s, C-2), 100.5 (d, C-3), 155.6 (s, C-4), 156.1 (s, C-5), 114.1 (d, C-6), 158.0 (s, C-7), 108.5 (d, C-8), 32.3 (t, C-9), 32.4 (t, C-10), 115.5 (s, C-4a), 143.0 (s, C-4b), 114.1 (s, C-8a), 143.9 (s, C-8b), 57.7 (q, 4-OMe)。以上数据与文献[14]报道基本一致,故鉴定该化合物3为2, 5, 7-三羟基-4-甲氧基-9, 10-二氢菲。
4, 7-二羟基-2, 3-二甲氧基-9, 10-二氢菲 (4, 7-Dihydroxy-2, 3-dimethoxy-9, 10-dihydrophenan-threne, 4) 无色块状晶体,ESI-MS m/z:[M + Na]+ 295,分子式C16H16O4。1H NMR (CD3OD, 500 MHz): δ 8.23 (1H, d, J=9.4 Hz, H-5), 6.68 (2H, m, H-6/8), 6.40 (1H, s, H-1), 3.83 (3H, s, 3-OMe), 3.81 (3H, s, 2-OMe), 2.66 (4H, s, H-9/10); 13C NMR (CD3OD, 125 MHz): δ 104.2 (s, C-1), 151.7 (d, C-2), 135.2 (s, C-3), 148.6 (s, C-4), 116.5 (s, C-4a), 126.3 (d, C-4b), 130.0 (s, C-5), 113.6 (s, C-6), 156.2 (d, C-7), 115.1 (d, C-8), 140.2 (q, C-8a), 31.3 (q, C-9), 31.5 (q, C-10), 136.3 (q, C-8b), 56.2 (q, 2-OMe), 62.0 (q, 3-OMe)。以上数据与文献[15]报道一致,故鉴定该化合物4为4, 7-二羟基-2, 3-二甲氧基-9, 10-二氢菲。
2, 5-二羟基-3, 4-二甲氧基-9, 10-二氢菲 (2, 5-Dihydroxy-3, 4-dimethoxy-9, 10-dihydrophenan-threne, 5) 褐色无定形粉末,ESI-MS m/z:[M + Na]+ 295,分子式C16H16O4。1H NMR (CDCl3, 500 MHz): δ 7.08 (1H, dd, J=7.50, 7.69 Hz, H-7), 6.69 (1H, d, J=7.50 Hz, H-6), 6.68 (1H, d, J=7.69 Hz, H-8), 3.87 (3H, s, 3-OMe), 3.68 (3H, s, 4-OMe), 2.64 (2H, m, H-9), 2.55 (2H, m, H-10); 13C NMR (CDCl3, 125 MHz): δ 113.7 (d, C-1), 150.3 (s, C-2), 138.3 (s, C-3), 151.1 (s, C-4), 118.6 (s, C-4a), 121.0 (s, C-4b), 154.4 (s, C-5), 119.8 (d, C-6), 129.1 (d, C-7), 119.2 (d, C-8), 32.2 (t, C-9), 31.6 (t, C-10), 61.7 (q, 3-OMe), 62.7 (q, 4-OMe)。以上数据与文献[16]报道基本一致,故鉴定该化合物5为2, 5-二羟基-3, 4-二甲氧基-9, 10-二氢菲。
2, 7-二羟基-3, 4, 6-三甲氧基-9, 10-二氢菲 (2, 7-Dihydroxy-3, 4, 6-trimethoxy-9, 10-dihydrophenan-threne, 6) 白色粉末,ESI-MS m/z: [M + Na]+ 325, 分子式C17H18O5。1H NMR (CDCl3, 500 MHz): δ 7.91 (1H, d, J=8.37 Hz, H-5), 6.73 (H, s, H-8), 6.84 (1H, m, H-1), 2.83 (4H, q, J=7.0 Hz, H-9/10),3.97 (3H, t, J=7.0, 3-OMe), 3.92 (3H, t, J=7.0 Hz, 4-OMe), 3.75 (3H, t, J=7.0 Hz, 6-OMe); 13C NMR (CDCl3, 125 MHz): δ 110.1 (d, C-1), 146.5 (s, C-2), 143.9 (s, C-3), 150.1 (s, C-4), 124.8 (s, C-4a), 131.0 (s, C-4b), 113.8 (d, C-5), 144.8 (s, C-6), 144.8 (s, C-7), 113.8 (d, C-8), 134.4 (s, C-8a), 128.9 (s, C-8b)。以上数据与文献[17]报道基本一致,故鉴定该化合物6为2, 7-二羟基-3, 4, 6-三甲氧基-9, 10-二氢菲。
(E) 松柏醛[(E)-Coniferylaldehye, 7] 黄色粉末,ESI-MS m/z: [M + H]+ 179,分子式C10H10O3。1H NMR (CDCl3, 500 MHz): δ 9.67 (1H, d, J=7.75 Hz, H-9), 7.41 (1H, d, J=15.8 Hz, H-7), 7.16 (1H, dd, J=1.90, 8.19 Hz, H-6), 7.09 (1H, d, J=1.90 Hz, H-2), 6.98 (1H, d, J=8.19 Hz, H-5), 6.64 (1H, dd, J=7.75, 15.8 Hz, H-8), 3.97 (3H, s, 3-OMe); 13C NMR (CDCl3, 125 MHz): δ 126.8 (s, C-1), 109.6 (d, C-2), 147.1 (s, C-3), 149.1 (s, C-4), 115.1 (d, C-5), 124.2 (d, C-6), 153.3 (d, C-7), 126.6 (d, C-8), 193.8 (d, C-9), 56.2 (q, 3-OMe)。以上数据与文献[18]报道基本一致,故鉴定该化合物7为 (E) 松柏醛。
反式对羟基肉桂酸酯 (trans-p-Hydroxylethyl cinnamate, 8) 无色晶体,ESI-MS m/z: [M + H]+ 193,分子式C11H12O3。1H NMR (CD3OD,500 MHz): δ 7.46 (2H, dd, J=8.6, 1.8 Hz, H-2/6), 7.43 (1H, d, J=15.6, 7.72 Hz, H-7), 6.81 (2H, dd, J=8.6, 1.8 Hz, H-3/5), 6.32 (1H, m, J=15.6 Hz, H-8), 4.22 (2H, q, J=7.17 Hz, H-10), 1.33 (3H, t, J=7.17 Hz, H-11); 13C NMR (CD3OD, 125 MHz): δ 127.1 (s, C-1), 131.1 (d, C-2/6), 116.8 (d, C-3/5), 161.4 (s, C-4), 146.4 (d, C-7), 115.2 (d, C-8), 169.4 (s, C-9), 61.4 (t, C-10), 14.6 (q, C-11)。以上数据与文献[19]报道一致,故鉴定该化合物8为反式对羟基肉桂酸酯。
对羟基苯丙酸甲酯 (p-Hydroxyphenylpropio nic methyl ester, 9) 无色油状,ESI-MS m/z:[M + Na]+ 203,分子式C10H12O3。1H NMR (CDCl3, 500 MHz): δ 7.10 (2H, d, J=8.3 Hz, H-2/6), 6.75 (2H, d, J=8.3 Hz, H-3/5), 3.68 (3H, s, -OCH3), 2.90 (2H, t, J=7.6 Hz, H-8), 2.59 (2H, t, J=7.6 Hz, H-7);13C NMR (CDCl3, 125 MHz): δ 132.0 (s, C-1), 129.6 (d, C-2/6), 115.4 (d, C-3/5), 154.3 (s, C-4), 30.3 (t, C-7), 36.4 (t, C-8), 173.3 (s, C-9), 51.0 (q, 9-OMe)。以上数据与文献[20]报道一致,故鉴定该化合物9为对羟基苯丙酸甲酯。
十二元内环酯 (Lasiodiplodin 10) 白色粉末,ESI-MS m/z:[M + Na]+ 301,分子式C16H22O4。1H NMR (CDCl3, 500 MHz): δ 6.25 (1H, d, J=1.9 Hz, H-14), 6.22 (1H, d, J=1.9 Hz, H-12), 5.32 (1H, m, H-3), 3.75 (3H, s, 15-OMe), 2.53 (2H, m, H-10), 1.25-2.18 (12H, m, H-4/5/6/7/8/9), 1.35 (3H, d, J=6.4 Hz, H-17); 13C NMR (CDCl3, 125 MHz): δ 169.2 (s, C-1), 72.4 (d, C-3), 32.4 (t, C-4), 21.4 (t, C-5), 26.5 (t, C-6), 24.3 (t, C-7), 25.6 (t, C-8), 30.2 (t, C-9), 30.5 (t, C-10), 143.1 (s, C-11), 108.5 (d, C-12), 158.0 (s, C-13), 97.1 (d, C-14), 158.0 (s, C-15), 117.3 (s, C-16), 19.6 (q, C-17), 55.9 (q, C-18)。以上数据与文献[21]报道基本一致,故鉴定该化合物10为十二元内环酯。
1.4 乙酰胆碱酯酶抑制活性根据Li等[22]方法测定化合物的乙酰胆碱酯酶 (AChE,Sigma公司) 抑制活性。将化合物1~10用DMSO溶解,配制成50 μg mL-1的待测样品。依次移取110 μL磷酸缓冲液 (PBS, pH 8.0)、10 μL待测样品和0.02 μg mL-1乙酰胆碱酯酶40 μL于96孔板中,在30℃下温育20 min后加入二硫二硝基苯甲 (Dithiobisnitrobenzoic acid,DTNB,2.48 g L-1,Sigma公司) 和碘化硫代丁酰胆碱 (Acetylthiocholine,ATch, Sigma公司,用50 mmol L-1 PBS配制,pH 8.0, 1.81 g L-1) 等体积混合液40 μL,于30℃下反应30 min,在405 nm波长下用酶标仪进行检测。阳性对照为他克林 (反应终浓度为0.333 μmol L-1),阴性对照为DMSO (终浓度为0.1%),每个样品同时做3个平行测试,取平均值。化合物对AChE的抑制率=(E-S)/E×100%,E为阴性对照的平均吸光值,S为待测样品的平均吸光值。
结果表明,化合物2、6、7和10对AChE的抑制率分别为25.32%、21.98%、53.10%和30.22%, 显示具有一定的抑制活性。
2 结果和讨论从华石斛中共分离得到10个化合物,分别是鼓槌石斛素 (1)、2′, 4′-二羟基查尔酮 (2)、2, 5, 7-三羟基-4-甲氧基-9, 10-二氢菲 (3)、4, 7-二羟基-2, 3-二甲氧基-9, 10-二氢菲 (4)、2, 5-二羟基-3, 4-二甲氧基-9, 10-二氢菲 (5)、2, 7-二羟基-3, 4, 6-三甲氧基-9, 10-二氢菲 (6)、(E) 松柏醛 (7)、反式对羟基肉桂酸酯 (8)、对羟基苯丙酸甲酯 (9) 和十二元内环酯 (10)。其中化合物1~2为联苄类化合物,化合物3~6为菲类化合物,化合物8~9为二苯苄类、菲类化合物合成的中药前体化合物[23]。此前陈秀娟等从华石斛茎中分离得到1个菲醌类化合物[24]和4个联苄类化合物[25],并且华石斛全草具有一定的抗氧化活性、抗肿瘤细胞活性和抗人体病原菌活性等。本研究在已有的理论基础上,丰富了华石斛的化学成分组成,也为以后研究提供了理论依据;另外,化合物2、6、7和10还具有一定的乙酰胆碱酯酶活性抑制活性。
| [1] |
Guangdong Institute of Botany.
Flora Hainannica, Tome 4[M]. Beijing: Science Press, 1977: 221-223.
广东省植物研究所. 海南植物志, 第4卷[M]. 北京: 科学出版社, 1977: 221-223. |
| [2] |
ZHANG G N, BI Z M, WANG Z T, et al. Advances in studies on chemical constitutents from plants of Dendrobium Sw.[J].
Chin Trad Herb Drugs, 2003, 34(6): 102-105. 张光浓, 毕志明, 王峥涛, 等. 石斛属植物化学成分研究进展[J]. 中草药, 2003, 34(6): 102-105. |
| [3] |
LI J, LI S X, HUANG D, et al. Advances in resources, constituents and pharmacological effects of Dendrobium officinale[J].
Sci Techn Rev, 2011, 29(18): 74-79. 李娟, 李顺祥, 黄丹, 等. 铁皮石斛资源、化学成分及药理作用研究进展[J]. 科技导报, 2011, 29(18): 74-79. DOI:10.3981/j.issn.1000-7857.2011.18.012 |
| [4] | MORITA H, FUJIWARA M, YOSHIDA N, et al. New picrotoxinin-type and dendrobine-type sesquiterpenoids from Dendrobium snow-flake 'Red star'[J]. Tetrahedron, 2000, 56(32): 5801-5805. DOI:10.1016/S0040-4020(00)00530-5 |
| [5] |
Chen X M, Wang C L, Yang J S, et al. Research progress on chemical composition and chemical analysis of Dendrobium officinale[J].
Chin Pharm J, 2013, 48(19): 1634-1639. 陈晓梅, 王春兰, 杨峻山, 等. 铁皮石斛化学成分及其分析的研究进展[J]. 中国药学杂志, 2013, 48(19): 1634-1639. |
| [6] |
Zhang X M, Sun Z R, Chen L, et al. Advances of studies on chemical constituents and pharmacological effect of Dendrobium nobile[J].
Chin J Mod Appl Pharm, 2014, 31(7): 895-899. 张晓敏, 孙志蓉, 陈龙, 等. 金钗石斛的化学成分和药理作用研究进展[J]. 中国现代应用药学, 2014, 31(7): 895-899. |
| [7] |
LI C Z, YU W Z, JIANG Y Y, et al. Protective effect of Dendrobium mixture on renal function of experimental diabetic rats[J].
J Fujian Univ TCM, 2012, 22(3): 18-21. 李长征, 余文珍, 蒋艺燕, 等. 石斛合剂对糖尿病大鼠肾脏的保护作用[J]. 福建中医药大学学报, 2012, 22(3): 18-21. DOI:10.3969/j.issn.1004-5627.2012.03.007 |
| [8] | XIA L Z, ZHOU M, XIAO Y H, et al. Chemical constituents from Helwingia japonica[J]. Chin J Nat Med, 2010, 8(1): 16-20. DOI:10.3724/SP.J.1009.2010.00016 |
| [9] |
SONG G Q, LIU X M, WANG Q, et al. Research progress on pharmacological activities of medical plants from Dendrobium Sw.[J].
Chin Trad Herb Drugs, 2014, 45(17): 2576-2580. 宋广青, 刘新民, 王琼, 等. 石斛药理作用研究进展[J]. 中草药, 2014, 45(17): 2576-2580. DOI:10.7501/j.issn.0253-2670.2014.17.028 |
| [10] | BHANDARI S R, KAPADI A H, MUJUMDER P L, et al. Nudol, a phenanthrene of the orchids Eulophia nuda, Eria carinata and Eria stricta[J]. Phytochemistry, 1985, 24(4): 801-804. DOI:10.1016/S0031-9422(00)84898-0 |
| [11] |
JIANG H Y, YANG F S, SONG X Q. Preliminary study on artifical sowing of Dendrobium sinense in natural habitat in Bawangling Nature Reserve, Hainan Island[J].
Trop For, 2011, 39(2): 40-43. 姜昊颖, 杨福孙, 宋希强. 华石斛原生境条件下人工播种的初步探讨[J]. 热带林业, 2011, 39(2): 40-43. DOI:10.3969/j.issn.1672-0938.2011.02.011 |
| [12] |
MA G X, XU G J, XU L S, et al. Studies on chemical constituents of Dendrobium chrysotoxum Lindl.[J].
Acta Pharm Sin, 1994, 29(10): 763-766. 马国祥, 徐国均, 徐珞珊, 等. 鼓槌石斛化学成分的研究[J]. 药学学报, 1994, 29(10): 763-766. |
| [13] |
YAO S Y, MA Y B, TANG Y, et al. Chemical constituents of Oxytropis falcate[J].
China J Chin Mat Med, 2008, 33(12): 1418-1421. 姚淑英, 马云保, 唐亚, 等. 镰形棘豆的化学成分研究[J]. 中国中药杂志, 2008, 33(12): 1418-1421. |
| [14] | HU J M, CHEN J J, YU H, et al. Five new compounds from Dendro-bium longicornu[J]. Planta Med, 2008, 74(5): 535-539. DOI:10.1055/s-2008-1074492 |
| [15] | KIM J H, OH S Y, HAN S B, et al. Anti-inflammatory effects of Dendrobium nobile derived phenanthrenes in LPS-stimulated murine macrophages[J]. Arch Pharmac Res, 2015, 38(6): 1117-1126. DOI:10.1007/s12272-014-0511-5 |
| [16] | ESTRADA S, TOSCANO R A, MATA R. New phenanthrene deri-vatives from Maxillaria densa[J]. J Nat Prod, 1999, 62(8): 1175-1178. DOI:10.1021/np990061e |
| [17] | PETTIT G R, SINGH S B, NIVEN M L, et al. Cell growth inhibitory dihydrophenanthrene and phenanthrene constituents of the African tree Combretum caffrum[J]. Can J Chem, 1988, 66(3): 406-413. DOI:10.1139/v88-071 |
| [18] | XIAN Y X, ZHOU H L, WANG X, et al. Chemical constituents of Gleditsia sinensis thorns[J]. Asian J Chem, 2015, 27(3): 1063-1065. DOI:10.14233/ajchem.2015.18240 |
| [19] |
ZHU H L, WANG Z Z, ZHENG B Z, et al. Chemical constituents from berries of Physalis pubescens[J].
Chin Trad Herb Drugs, 2016, 47(5): 732-735. 朱海林, 王振洲, 郑炳真, 等. 毛酸浆果实的化学成分研究[J]. 中草药, 2016, 47(5): 732-735. DOI:10.7501/j.issn.0253-2670.2016.05.007 |
| [20] |
LIU D L, PANG F G, ZHANG J X, et al. Studies on the chemical constituents of Bulbophyllum odoratissimum Lindl.[J].
Chin J Med Chem, 2005, 15(2): 103-107. 刘岱琳, 庞发根, 张家欣, 等. 密花石豆兰的化学成分研究[J]. 中国药物化学杂志, 2005, 15(2): 103-107. DOI:10.3969/j.issn.1005-0108.2005.02.011 |
| [21] | WANG H S, WANG Y H, SHI Y N, et al. Chemical constituents in roots of Osbeckia opipara[J]. China J Chin Mat Med, 2009, 34(4): 414-418. DOI:10.3321/j.issn:1001-5302.2009.04.011 |
| [22] | LI W, CAI C H, GUO Z K, et al. Five new eudesmane-type sesqui-terpenoids from Chinese agarwood induced by artificial holing[J]. Fitoterapia, 2015, 100: 44-49. DOI:10.1016/j.fitote.2014.11.010 |
| [23] | CROMBIE L, CROMBIE W M L. Natural products of Thailand high Δ1-thc-strain Cannabis, the bibenzyl-spiran-dihydrophenanthrene group: Relations with cannabinoids and canniflavones[J]. J Chem: Perkin Trans, 1982: 1455-1466. DOI:10.1039/P19820001455 |
| [24] | CHEN X J, MEI W L, ZUO W J, et al. A new antibacterial phenan-threnequinone from Dendrobium sinense[J]. J Asian Nat Prod Res, 2013, 15(1): 67-70. DOI:10.1080/10286020.2012.740473 |
| [25] | CHEN X J, MEI W L, CAI C H, et al. Four new bibenzyl derivatives from Dendrobium sinense[J]. Phytochem Lett, 2014, 9(1): 107-112. DOI:10.1016/j.phytol.2014.04.012 |
 2017, Vol. 25
2017, Vol. 25



